Objetivos:
Terminada la lección podrás:
- Explicar los eventos biográficos de Ernest Rutherford.

Introducción
Ernest Rutherford: El Padre de la Física Nuclear y su Revolución en la Comprensión del Átomo
En el panteón de los grandes científicos que transformaron nuestra comprensión del mundo, Ernest Rutherford ocupa un lugar de honor. Este físico y químico neozelandés, galardonado con el Premio Nobel de Química en 1908, no solo desentrañó los misterios de la radiactividad, sino que, a través de sus ingeniosos experimentos, demolió las nociones preexistentes sobre el átomo, sentando las bases de la física nuclear moderna.
Su trabajo pionero nos reveló un universo subatómico de una complejidad y elegancia inimaginables, cambiando para siempre el curso de la ciencia.
¿Quién fue Ernest Rutherford?
Ernest Rutherford (1871-1937) fue un brillante físico y químico neozelandés, considerado uno de los padres fundadores de la física nuclear y atómica. Desde temprana edad, mostró una excepcional aptitud para la ciencia, lo que lo llevó a estudiar en la Universidad de Canterbury en Nueva Zelanda. Posteriormente, obtuvo una beca para el Laboratorio Cavendish de la Universidad de Cambridge, donde trabajó bajo la tutela de J.J. Thomson, el descubridor del electrón.
La carrera de Rutherford se caracterizó por su enfoque experimental riguroso y su capacidad para interpretar resultados que desafiaban las teorías establecidas. A lo largo de su vida, ocupó importantes cargos académicos, incluyendo cátedras en la Universidad McGill en Canadá y la Universidad de Manchester, antes de regresar a Cambridge como director del Laboratorio Cavendish, sucediendo a su antiguo mentor, J.J. Thomson.
La Radiactividad: Sus Descubrimientos Fundamentales
El descubrimiento de la radiactividad por Henri Becquerel en 1896 abrió un campo completamente nuevo de investigación. Rutherford se sumergió en este fenómeno, realizando contribuciones decisivas:
Identificación de los tipos de radiación (1899):
Rutherford fue el primero en demostrar que la radiación emitida por sustancias como el uranio no era un fenómeno simple, sino que consistía en al menos dos tipos distintos de “rayos”, a los que llamó:
- Rayos Alfa (α): Demostró que tenían carga positiva y que eran partículas relativamente pesadas. Más tarde, los identificó como núcleos de helio (dos protones y dos neutrones). Estas partículas tienen un bajo poder de penetración.
- Rayos Beta (β): Descubrió que tenían carga negativa y una masa mucho menor que las partículas alfa, identificándolos como electrones de alta energía. Tenían un poder de penetración mayor que las partículas alfa.
Posteriormente, Paul Villard descubrió los rayos Gamma (γ), que Rutherford también investigó, confirmando que eran radiación electromagnética de alta energía y sin carga, con un poder de penetración muy elevado.
Teoría de la Desintegración Radiactiva (1902, con Frederick Soddy):
Propuso que la radiactividad era el resultado de la transmutación espontánea de los elementos. Es decir, los átomos de elementos radiactivos se desintegran o “decaen” con el tiempo, transformándose en átomos de otros elementos mientras emiten radiación. Esta teoría revolucionaria contradijo la idea de que los átomos eran indivisibles e inmutables, abriendo el campo de la física nuclear.
Concepto de Vida Media:
A partir de la desintegración radiactiva, Rutherford introdujo el concepto de vida media, que es el tiempo que tarda la mitad de una muestra de un elemento radiactivo en desintegrarse.
Su Percepción del Átomo: El Modelo Nuclear
La contribución más famosa de Rutherford a nuestra comprensión del átomo surgió de su “experimento de la lámina de oro” (1911), realizado con sus colaboradores Hans Geiger y Ernest Marsden. En ese momento, el modelo atómico predominante era el “modelo del pudín de pasas” de J.J. Thomson, que postulaba que el átomo era una esfera de carga positiva uniformemente distribuida con electrones negativos incrustados en ella.
Experimento
El experimento consistió en bombardear una delgada lámina de oro con partículas alfa. Según el modelo de Thomson, se esperaba que las partículas alfa pasaran a través de la lámina con solo una ligera desviación. Sin embargo, los resultados sorprendieron a Rutherford:
- La gran mayoría de las partículas alfa atravesaron la lámina sin desviarse o con una desviación mínima, lo que indicaba que el átomo era en su mayor parte espacio vacío.
- Una pequeña fracción de las partículas alfa (aproximadamente 1 de cada 8.000) fueron desviadas en ángulos muy grandes, e incluso algunas rebotaron hacia atrás, como si hubieran chocado con algo muy denso y cargado positivamente.
Modelo atómico
A partir de estos resultados, Rutherford formuló un nuevo modelo atómico, el modelo atómico de Rutherford (también conocido como modelo planetario o nuclear):
- Núcleo Atómico: La mayor parte de la masa y toda la carga positiva del átomo se concentra en una región central extremadamente pequeña y densa, a la que llamó núcleo.
- Electrones Orbitantes: Los electrones (con carga negativa y una masa insignificante) giran alrededor de este núcleo en órbitas, de manera similar a como los planetas orbitan alrededor del Sol.
- Átomo Mayormente Vacío: Debido al pequeño tamaño del núcleo y la vasta extensión de las órbitas electrónicas, el átomo es, en su mayoría, espacio vacío.
- Carga Neutra: El número de electrones es igual a la carga positiva del núcleo, haciendo que el átomo sea eléctricamente neutro.
Limitaciones
Aunque el modelo de Rutherford tenía limitaciones (no podía explicar por qué los electrones no caían en espiral hacia el núcleo al irradiar energía), fue un avance gigantesco que sentó las bases para el modelo de Bohr y, en última instancia, para la mecánica cuántica. Su descubrimiento del núcleo atómico es considerado uno de los logros más importantes de la física del siglo XX.
Conclusión
Ernest Rutherford no fue solo un físico excepcional, sino un arquitecto fundamental de nuestro conocimiento sobre la estructura más íntima de la materia. Sus investigaciones pioneras sobre la radiactividad no solo revelaron la naturaleza de las emisiones nucleares, sino que también demostraron que los átomos no eran partículas indivisibles, sino entidades dinámicas capaces de transformarse. Su icónico experimento de la lámina de oro y la consiguiente postulación del núcleo atómico representaron un cambio de paradigma radical, transformando nuestra percepción del átomo de una esfera uniforme a un sistema planetario en miniatura.
El legado de Rutherford es incalculable; es el padre de la física nuclear, y sus descubrimientos no solo abrieron las puertas a la comprensión de las fuerzas fundamentales, sino que también sentaron las bases para el desarrollo de la energía nuclear, la medicina nuclear y, en última instancia, toda la física de partículas.
Otras biografías en este website
- Aristarco de Samos un Pensador
- Biografías
- Biografías de Científicos Destacados
- Erwin Scrödinger su Gato y Biografía
- Hipócrates de Cos: Antiguo Médico
- Henry Cavendish y la Densidad
- Isaac Newton y la Física
- James Clerk Maxwell, Físico y Matemático
- Johannes Kepler y sus Leyes
- Nicolás Copérnico: Teoría Heliocéntrica
- Robert Hooke, Hombre del Renacimiento
- Sir William Herschel y las Galaxias
Enlaces externos para explorar
Simulación
Núcleo atómico
Dispersión
Experimento de Rutherford
Vídeo
Páginas recientes
- Carl Friedrich Gauss: Matemática y Física
- La IA Revoluciona la Investigación
- Ernest Rutherford y su Legado
- Antoine Henri Becquerel y la Radiactividad
- La Ocultación en Astronomía
- Escribiendo el Póster de la Investigación
- Presentando la Investigación – Poster
- Movimiento de Traslación en el Universo
- Movimiento de Rotación en el Universo
- Webquest: Explorando el Universo
- Metodo, Procedimiento e Investigación
- Maria Skłodowska-Curie y la Radiactividad
- Investigando el Desplazamiento de Wien
- El Hielo, la Nieve y la Lluvia Helada
- Niels Bohr y la Estructura Atómica
Más páginas para explorar
-

¡Vistiendo para el Espacio!
-

Abstract: Resumen Breve de Investigación
-

Aceleración en Caída Libre
-

Aceleración Grativacional en Planetas
-

Aceleración Gravitacional en la Tierra
-

Aceleración Lineal y sus Representaciones
-

Aisladores y Conductores
-

Alacena virtual de conversiones
-
Albert Einstein Historia y Vida
-
Alessandro Volta y la Electricidad
-

Amedeo Avogadro y su Ley
-
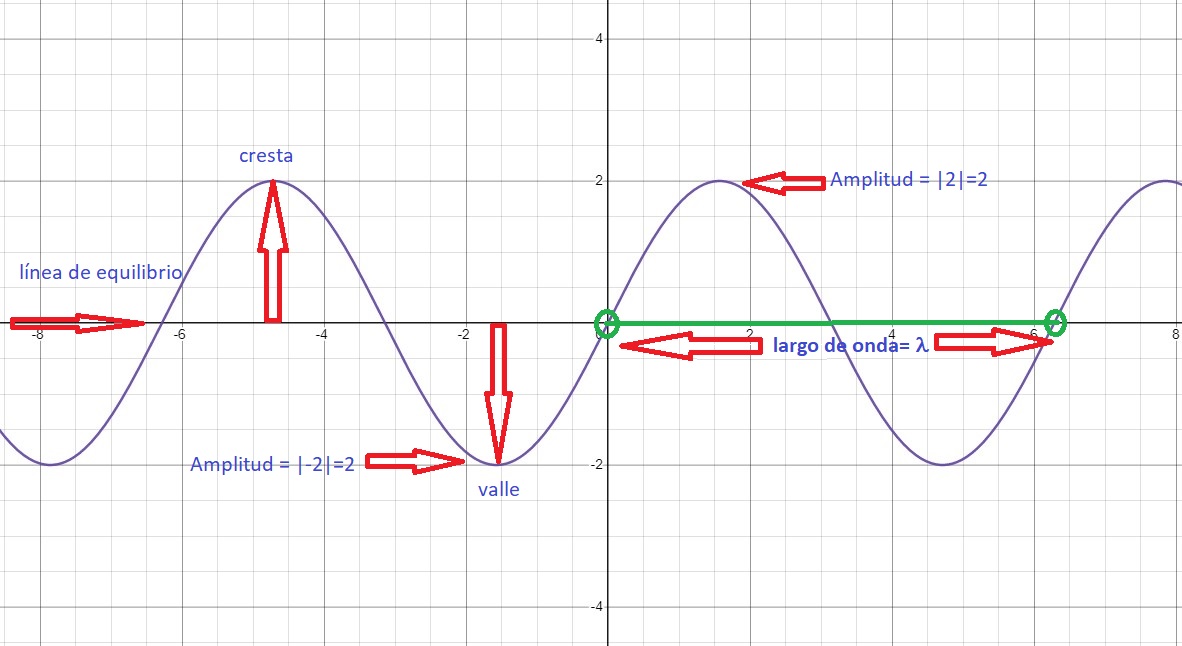
Amplitud, largo de onda y frecuencia
-

Análisis Gráfico del Movimiento
-

Andrés Ampere y el Electromagnetismo
-

Antoine Henri Becquerel y la Radiactividad
-

Ernest Rutherford y su Legado
-

Antoine Henri Becquerel y la Radiactividad
-
La Ocultación en Astronomía













